中国组织工程研究 ›› 2013, Vol. 17 ›› Issue (51): 8875-8880.doi: 10.3969/j.issn.2095-4344.2013.51.015
• 材料生物相容性 material biocompatibility • 上一篇 下一篇
羟基磷灰石表面修饰人工角膜钛支架的生物相容性
马 骁1,石 红1,黄一飞2,黄靖香2,崔福斋3
- 1北京世纪坛医院眼科,北京市 100038;2解放军总医院眼科,北京市 100853;3清华大学材料科学工程系,北京市 100084
Biocompatibility of hydroxyapatite modified titanium skirt for keratoprosthesis
Ma Xiao1, Shi Hong1, Huang Yi-fei2, Huang Jing-xiang2, Cui Fu-zhai3
- 1 Department of Ophthalmology, Hospital of Shijitan, Beijing 100038, China; 2 Department of Ophthalmology, General Hospital of PLA, Beijing 100853, China; 3 Department of Materials Science and Engineering, Tsinghua University, Beijing 100084, China
摘要:
背景:纯钛作为安全的生物种植体材料已被用于制作俄罗斯钛人工角膜,但其临床使用中仍存在人工角膜移位、漏水、角膜组织融解或人工角膜排出等并发症。 目的:观察经羟基磷灰石表面修饰人工角膜钛支架在碱烧伤兔角膜内的生物相容性。 方法:将30只右眼角膜碱烧伤新西兰白兔随机分为3组,实验组于角膜基质层内植入经羟基磷灰石表面修饰的人工角膜钛支架,对照组于角膜基质层内植入人工角膜钛支架,空白对照组仅作角膜板层切口。 结果与结论:所有支架在观察期内稳定存留,无角膜坏死融解及支架脱出发生。术后2,8周,实验组与对照组炎症细胞浸润数量明显高于空白对照组(P < 0.05),16周后各组间炎症细胞浸润数量差异无显著性意义。术后2,8,16周,实验组角膜成纤维细胞数高于对照组和空白对照组(P < 0.05)。实验组支架表面有密集的角膜细胞及细胞外基质紧密抓附,支架与角膜组织愈合良好;对照组支架表面仅见少量角膜组织简单包裹,支架与角膜组织未真正愈合。表明羟基磷灰石表面修饰的人工角膜钛支架可在碱烧伤兔角膜组织中稳定存留,生物相容性较单纯钛支架提高。
中图分类号:


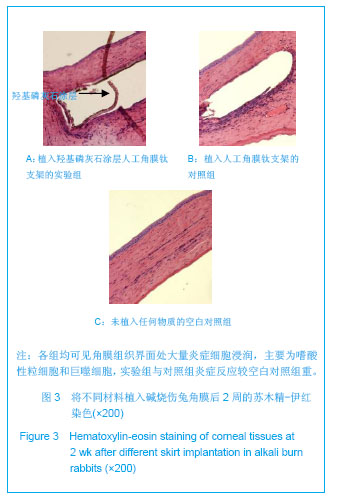





.jpg)